周期8周
费用100000
资料基本资料
机构SUNGO
产品医疗用品
2017 年4 月5 日,欧洲议会和理事会正式签发了欧盟关于器械第2017/七45 号法规(MDR,EU2017/七45),5月5日,欧盟(Official Journal of the EuropeanUnion) 正式发布该法规。2017 年5 月25 日,MDR 正式生效, 替代了原器械指令(MDD,93/42/EEC)和主动植入式器械指令(AIMD,90/385/EEC)。
欧盟会规定了MDR 的转换期的要求
2017 年5 月25 日:MDR 和IVDR 生效
2020 年3 月25 日:启动欧盟器械数据库(Eudamed)
2021 年5 月25 日:MDR 实施开始
2022 年5 月25 日:IVDR 实施开始
2024 年5 月25 日:AIMD,MDD 和IVDD 证将失效
按产品的危险程度,将产品分为Ⅰ类、Is(灭菌),Im(测量),Ⅱa类、Ⅱb类、Ⅲ类
对于目前MDD和MDR的各个风险等级的产品实施时间:
1. 对于I类的产品,欧盟强制要求2021年5月25号强制实施MDR
2. 对于Is(灭菌),Im(测量),Ⅱa类、Ⅱb类、Ⅲ类迟可以用到2024年5月25号
3.对于可重复使用的产品,在MDD里属于I类,但是在MDR里属于Ir类,那么如果企业在2021年5月25号之前满足了MDD的要求,迟可以用到2024年5月25号

目前急需做CE认证的客户很多,检测认证公司,代理公司也是鱼目混
杂,参差不齐。
怎么辨别口罩CE认证的真假呢?
1,凡是说3、5两千可以出CE证的都是
2,凡是说3/2天可以*的都是
3,凡是说国内公司自己可以发CE证的都是
辨别证的真伪很重要,因为一旦货到了港口清不了关损失就大了。
所以不要贪图*和快而上当受
NB号的CE证。按照现行的欧盟器械法规,此路径获取CE证的
时间至少8个月以上,费用比较昂贵。
欧盟I类器械,如果是非灭菌产品,具体分类为I类。按照指令要求,
公告机构不可强制介入I类器械的发证事宜,制造商可以基于完整的CE技
术文档宣称符合CE(自我CE符合性声明格式如下)。也即,制造商不需
要找发证机构去申请带NB号的CE证,制造商根据自己出具自我CE符
合性声即可打上CE mark,出口欧盟。在欧盟有经销活动前,需要委托
欧盟授权代表去当地主管机构做欧盟注册,整个欧盟28个成员国,只需
登记一次。整个周期是1-4周。
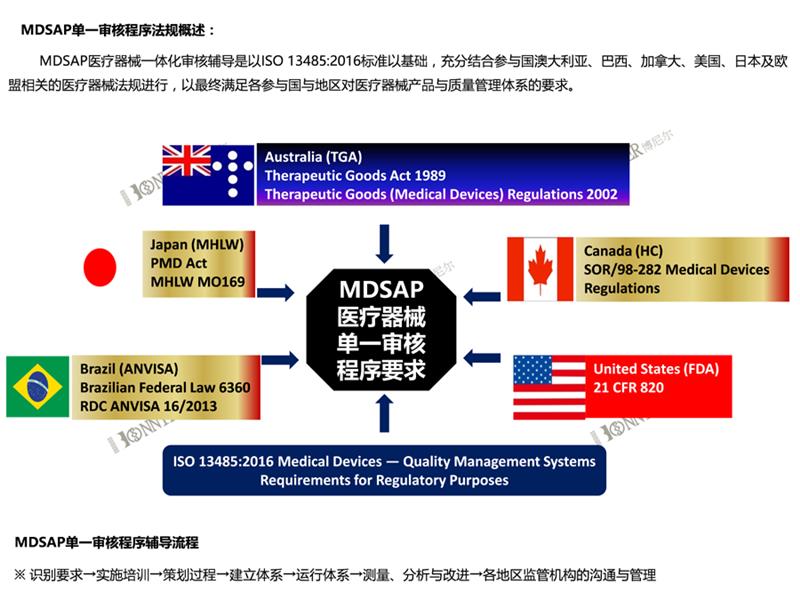
1.欧盟(非无菌):医用口罩、面罩、眼罩、防护服、隔离服和手套等非灭菌I类产品与检测试剂盒产品,提供技术文件、欧盟授权代表和注册凭证证办理服务。
备注:欧盟对于I类的产品,要求企业自己必须确保自己的产品符合欧盟法规,产品是*有效的,并建立相关技术文件,签署符合性声明,确定欧盟授权代表,然后到成员国主管当局注册登记之后,即可在产品加贴CE标志进入欧盟销售。
不需要公告机构参与审核发证的
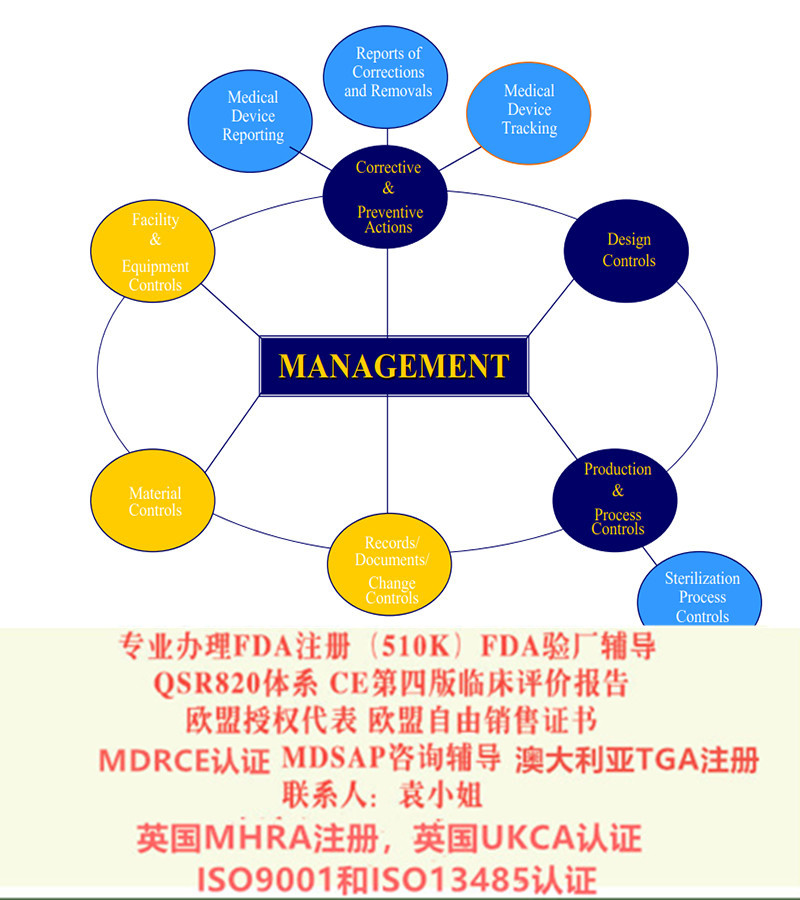
I类无菌器械:
若产品是I类无菌器械,则需要公告机构介入,有一个较长的审核周期。
I类无菌器械销往欧盟要求:
1. 编制产品技术文档
2. 建立ISO13485体系
3. 产品送检,取得产品检测报告
4. 接受公告机构的现场质量体系审核和技术文档审查
5. 获得具备相应的公告机构出具的CE认证证
6. 由欧代在其所在欧盟成员国主管当局(如CIBG、MHRA)进行信息注册并保存制造商的技术文档副
7. 在产品包装、标签上标记带有公告机构号的CE标志
加强警戒和市场监管,一旦器械可以在市场上使用,制造商将必须收集有关其性能的数据,欧盟国家将在市场监管领域进行更密切的协调。
http://sungofda.cn.b2b168.com